
В Україні ліцензування фармпрепаратів лише частково відповідає міжнародним стандартам – асоціація

НАБУ та ГПУ провели обшуки в рамках розслідування злочинів проти Майдану

Сніжна Україна на фото користувачів соціальних мереж
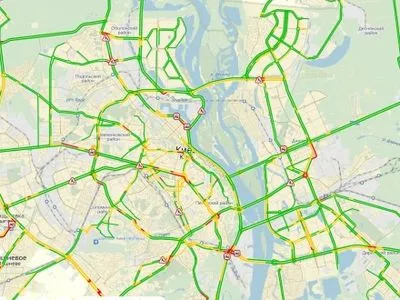
Затори у Києві сягнули шести балів

Головна ялинка Рівного буде висотою у 25 метрів

Суд по обранню запобіжного заходу директору нічного клубу у Львові продовжиться завтра

Держава щороку виділяє лише 10% від потреби на лікування онкохворих – В.Сердюк

Незаконне переміщення понад 1,3 тонни пряжі виявили на Одещині

У Києві презентували логотип і талісман Чемпіонату світу з хокею

Наступного тижня ВР розгляне подання про зняття недоторканості з В.Новинського – В.Арешонков
Популярні

У Харкові пролунав вибух

Лінії для голосування на Євробаченні 2024 відкриті: Голосуйте за свого фаворита через додатки або телефон

AVROTROS проти дискваліфікації Йоста Кляйна з Євробачення-2024: Заява щодо серйозності інциденту

Вогнеборці запобігли поширенню лісової пожежі на Харківщині в умовах ворожих обстрілів

Укрзалізниця вимикає підсвітку на найбільших вокзалах у години пік для економії електроенергії
Публікації

Російський слід бачать тільки боржники: як ярлик співпраці з рф використовують у бізнес-війнах

Проти в.о. заступника голови ДПС Сокура відкрита кримінальна справа через перешкоджання забезпеченню пальним армії

Кредитний лабіринт: як повернути кредит, коли ніхто в цьому не зацікавлений та має зовсім інші плани

Відкриття власного бізнесу як шлях адаптації ветеранів у цивільному житті: з якими проблемами стикаються колишні військові

Слабка ланка: хто в регіонах тягне на дно партію Юлії Тимошенко
В Україні ліцензування фармпрепаратів лише частково відповідає міжнародним стандартам – асоціація
Ліцензування фармацевтичних препаратів в Україні частково лише відповідає міжнародним стандартам. Про це у коментарі УНН повідомила Асоціація виробників інноваційних ліків “АПРаД”.

НАБУ та ГПУ провели обшуки в рамках розслідування злочинів проти Майдану
Співробітники Національного антикорупційного бюро України та слідчі Департаменту спеціальних розслідувань Генеральної прокуратури України провели понад десяток обшуків у регіонах країни в рамках розслідування кримінального провадження щодо злочинів проти Майдану. Про це УНН повідомили у прес-службі НАБУ.

Сніжна Україна на фото користувачів соціальних мереж
В Україну прийшла справжня зима. Користувачі у соцмережах діляться фотографіями засніжених вулиць, передає УНН.

Затори у Києві сягнули шести балів
Автомобільні затори у Києві сягнули шести балів, передає УНН з посиланням на “Яндекс-карти”.

Головна ялинка Рівного буде висотою у 25 метрів
Комунальники обрали новорічну ялинку, яка прикрашатиме центр Рівного. Цьогорічне дерево буде 25 метрів заввишки - на 1 метр вище, ніж торішня, повідомили УНН у інформаційному відділі Рівненському міськвиконкомі.

Суд по обранню запобіжного заходу директору нічного клубу у Львові продовжиться завтра
Сьогодні почали обирати запобіжний захід директору нічного клубу у Львові, в якому сталась пожежа. Наразі суд пішов у нарадчу кімнату, передає кореспондент УНН.

Держава щороку виділяє лише 10% від потреби на лікування онкохворих – В.Сердюк
На сьогодні у світі немає жодної цивілізованої країни, де онкохворі лікуються за власний кошт. Про це УНН повідомив Президент Всеукраїнської ради захисту прав та безпеки пацієнтів Віктор Сердюк.

Незаконне переміщення понад 1,3 тонни пряжі виявили на Одещині
Правоохоронці виявили 1,3 тонни пряжі у вантажівці, яка прямувала з Туреччини до України через пункт пропуску “Рені-Джурджулєшти” митного поста “Ізмаїл”. Про це УНН повідомили у прес-службі ДФС України.

У Києві презентували логотип і талісман Чемпіонату світу з хокею
У столичному Палаці Спорту презентували логотип і талісман Чемпіонату світу з хокею, який відбудеться в Україні в 2017 році, передає кореспондент УНН.

Наступного тижня ВР розгляне подання про зняття недоторканості з В.Новинського – В.Арешонков
Наступного тижня Верховна Рада може розглянути подання Генеральної прокуратури про надання згоди на притягнення до кримінальної відповідальності народного депутата Вадима Новинського. Про це сказав в ефірі "112 Україна" заступник голови комітету парламенту з питань регламенту та організації роботи ВР Володимир Арешонков, передає УНН.































